У водорода больше общего с щелочными металлами, чем казалось ранее
Впервые исследователи продемонстрировали, что водород может замещать щелочные металлы в типичных для этих s-элементов структурах.
Водород, на орбиталях которого расположен только один s-электрон, можно считать химическим аналогом щелочных металлов, электронная формула которых описывается формулой ns1. Однако при обычных условиях химические свойства водорода и щелочных металлов значительно различаются.
Это наглядно демонстрируется тем, что водород представляет собой газообразное вещество, а другие а элементы I группы ведут себя себя как химически активные металлы, которые при комнатной температуре и нормальном давлении являются твердыми веществами.
Несмотря на то, что можно отметить некоторое сходство водорода с щелочными металлами, в особенности с самым маленьким и легким их представителем – литием, связи в соединениях которого обладают наиболее ярко выраженным ковалентным характером химических связей, твердотельные соединения, в которых бы вместо щелочного металла содержался водород, до настоящего времени не были получены.
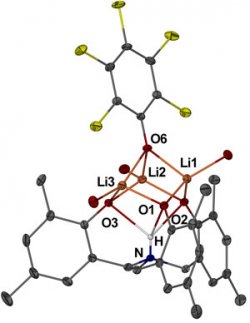
Водород может заместить литий в кубановом фрагменте фенолята этого щелочного металла (Рисунок из Chem. Commun., 2013, DOI: 101.1039/c3cc47393g)
На сегодняшний день Мэтью Дэвидсон (Matthew Davidson) с коллегами из Университета Бат в Великобритании разработал концепцию металлоорганического синтеза по созданию псевдокубановых фрагментов, с помощью трис(фенол)аминовых лигандов и атомов лития или натрия, причем в таком псевдокубановом фрагменте которых один из атомов металла замещается на атом водорода.
Водород образует редко представленную в химической литературе трифуркационную (разветвленную в трех направлениях) 4-х центровую водородную связь. Такой тип расположения не является необычной для щелочных металлов, которые, будучи более объемными, могут «позволить себе» принимать большие значения координационных чисел, однако для водорода такой тип структуры не является выгодным.
Дэвидсон говорит, что интересы исследовательской группы лежат в лучшем понимании того, как трис(фенол)аминовые лиганды можно применить для контроля за химически активными металлическими центрами. Доскональное понимание закономерностей координационной химии и способность обрисовать принципиальное сходство между химической активностью водорода и металлов в качестве кислот Льюиса смогло бы помочь в развитии таких областей как органокатализ.
Специалист по химии неорганических материалов Доминик Райт (Dominic Wright) из Кембриджского университета в Великобритании в восторге от проведенной исследователями работы.
Райт считает, что элегантная демонстрация того, что у ионов H+ все же есть определенное сходство с ионами щелочных металлов, благодаря которому ион водорода может заменить в ионы лития и натрия в твердотельных соединениях может стать основой для новых работ как в области молекулярной, так и супрамолекулярной химии.
Эту работу можно считать своего рода доказательством в пользу классического расположения водорода в качестве первого элемента первой группы, однако вряд ли сможет поставить точку в старой дискуссии, второй точкой зрения которой является то, что водород должен быть «заглавным» элементом группы галогенов.
Водород, на орбиталях которого расположен только один s-электрон, можно считать химическим аналогом щелочных металлов, электронная формула которых описывается формулой ns1. Однако при обычных условиях химические свойства водорода и щелочных металлов значительно различаются.
Это наглядно демонстрируется тем, что водород представляет собой газообразное вещество, а другие а элементы I группы ведут себя себя как химически активные металлы, которые при комнатной температуре и нормальном давлении являются твердыми веществами.
Несмотря на то, что можно отметить некоторое сходство водорода с щелочными металлами, в особенности с самым маленьким и легким их представителем – литием, связи в соединениях которого обладают наиболее ярко выраженным ковалентным характером химических связей, твердотельные соединения, в которых бы вместо щелочного металла содержался водород, до настоящего времени не были получены.
Водород может заместить литий в кубановом фрагменте фенолята этого щелочного металла (Рисунок из Chem. Commun., 2013, DOI: 101.1039/c3cc47393g)
На сегодняшний день Мэтью Дэвидсон (Matthew Davidson) с коллегами из Университета Бат в Великобритании разработал концепцию металлоорганического синтеза по созданию псевдокубановых фрагментов, с помощью трис(фенол)аминовых лигандов и атомов лития или натрия, причем в таком псевдокубановом фрагменте которых один из атомов металла замещается на атом водорода.
Водород образует редко представленную в химической литературе трифуркационную (разветвленную в трех направлениях) 4-х центровую водородную связь. Такой тип расположения не является необычной для щелочных металлов, которые, будучи более объемными, могут «позволить себе» принимать большие значения координационных чисел, однако для водорода такой тип структуры не является выгодным.
Дэвидсон говорит, что интересы исследовательской группы лежат в лучшем понимании того, как трис(фенол)аминовые лиганды можно применить для контроля за химически активными металлическими центрами. Доскональное понимание закономерностей координационной химии и способность обрисовать принципиальное сходство между химической активностью водорода и металлов в качестве кислот Льюиса смогло бы помочь в развитии таких областей как органокатализ.
Специалист по химии неорганических материалов Доминик Райт (Dominic Wright) из Кембриджского университета в Великобритании в восторге от проведенной исследователями работы.
Райт считает, что элегантная демонстрация того, что у ионов H+ все же есть определенное сходство с ионами щелочных металлов, благодаря которому ион водорода может заменить в ионы лития и натрия в твердотельных соединениях может стать основой для новых работ как в области молекулярной, так и супрамолекулярной химии.
Эту работу можно считать своего рода доказательством в пользу классического расположения водорода в качестве первого элемента первой группы, однако вряд ли сможет поставить точку в старой дискуссии, второй точкой зрения которой является то, что водород должен быть «заглавным» элементом группы галогенов.
| Источник: | Собственная информация |
| Учетная запись: | himsite.ru |
| Дата: | 14.11.13 |